Artículo Original
Efecto comparado de dosis inmunoestimulantes de fracciones ribosomales y proteoglicanos de membrana sobre la activación de subpoblaciones de células mononucleadas humanas de sangre periférica
Texca Tatevari Méndez-López, Alain Raimundo Rodríguez-Orozco, Carlos Béjar Lozano
ARCHIVOS DE ALERGIA E INMUNOLOGÍA CLÍNICA 2012;( 1):0010-0014 | DOI: 10.53108/AAIC/20121/0010-0014
Antecedentes. La población mexicana presenta una alta prevalencia de infecciones recurrentes de vías respiratorias altas.
Objetivos. Comparar el efecto de dosis inmunoestimulantes de ribosomas bacterianos y proteoglicanos de membrana Ribovac® sobre células mononucleadas.
Material y métodos. La expresión de IL-6 de células mononucleadas en cultivo, se midió a concentraciones y tiempos variables por la técnica de ELISA, mientras que el efecto de Ribovac® en poblaciones de células mononucleadas fue analizado por citometría de flujo.
Resultados. Ribovac® tiene un efecto dependiente de dosis y tiempo de exposición sobre la expresión de IL-6 por células mononucleadas; las concentraciones de IL-6 fueron máximas a las 6 horas de tratamiento con Ribovac®. La expresión de CD3+ fue mayor cuando las células mononucleadas se trataron con 125 μg/ml por 72 horas (p=0,010) respecto a aquellas que se trataron a mitad de esa concentración en igual tiempo, a diferencia de la expresión de CD19, que fue mayor en células mononucleadas tratadas con 62,5 μg/ml por 72 horas que en aquellas tratadas con 125 μg/ml por 72 horas (p=0,021). No se encontraron disminuciones estadísticamente significativas en el número de células CD16+CD56+ ni en la coexpresión de los marcadores CD45 y CD19 cuando se compararon tanto tiempos de administración como concentraciones de Ribovac®.
Conclusiones. La expansión de poblaciones linfoides y la maduración de éstas a fenotipos con mayor capacidad efectora son efectos inducibles y deseables de Ribovac®, que deben tenerse en cuenta al decidir su tiempo e intervalos de administración.
Palabras clave: ribosomas bacterianos, proteoglicanos de membrana, infecciones respiratorias recurrentes, inmunoestimulación, células mononucleadas, CD3, CD19, CD45, CD16 CD56, CD19, IL-6, Ribovac, Ribomunyl, Immunocytal.
Background. The Mexican population has a high prevalence of recurrent infections of upper respiratory tract.
Objective. To compare the effect of immunostimulatory dose of bacterial ribosomes and membrane proteoglycan Ribovac® on mononuclear cells.
Methods. The expression of interleukin 6 from mononuclear cells in culture was measured at varying concentrations and times by ELISA, while the effect of R in populations of mononuclear cells was analyzed by flow cytometry.
Results. Ribovac® has an dose-dependent and exposure time effect on the expression of IL-6 by mononuclear cells, concentrations of IL-6 were maximal at 6 hours of treatment with Ribovac®. The expression of CD3+ was higher when mononuclear cells were treated with 125 μg/ml for 72 hours (p=0,010) than those who were treated to half that concentration in the same time, unlike the expression of CD19 which was higher in mononuclear cells treated with 62,5 μg/ml for 72 hours than those that were treated with 125 μg/ml for 72 hours (p=0,021). There were no statistically significance in the decrease in the number of CD16+CD56+ cells and in the coexpression of CD45 and CD19 markers neither; when comparing both times of administration and evaluated concentrations of Ribovac®.
Conclusions. The lymphoid population expansion and their maturation to better effector phenotypes effector are inducible and desirable effects of Ribovac® and these important when deciding the time and intervals of administration.
Keywords: bacterial ribosomes, membrane proteoglycans, recurrent respiratory infections, immune stimulation, mononuclear cells, CD3, CD19, CD45, CD16 CD56, CD19, interleukin 6, Ribovac, Ribomunyl, Immunocytal.
Los autores declaran no poseer conflictos de intereses.
Fuente de información Asociación Argentina de Alergia e Inmunología Clínica. Para solicitudes de reimpresión a Archivos de Alergia e Inmunología Clínica hacer click aquí.
Recibido | Aceptado | Publicado
Introducción
Las infecciones respiratorias agudas constituyen la primera causa de consultas médicas y de morbilidad, tanto en los países desarrollados como en los países en vías de desarrollo. A pesar que las infecciones agudas de las vías respiratorias bajas concentran habitualmente la atención por su mayor complejidad, costo del tratamiento y complicaciones, son las infecciones de las vías respiratorias altas las que se presentan en mayor número en la consulta ambulatoria.
Las infecciones recurrentes de las vías respiratorias altas (IRVRA) en su mayoría tienen evolución favorable y ayudan a desarrollar el sistema inmunológico de los niños, aunque para la familia representan motivo de preocupación y ansieda.1,2 Algunos de los tratamientos potenciales o estrategias para reducir el número y costo de las IRVRA se basa en el uso de bacterias y extractos de bacterias para la inmunoterapia,3,4 gracias, en parte, a la identificación de moléculas originarias de los microorganismos que pueden ser reconocidas por receptores muy específicos expresados en diferentes estirpes celulares5,6 lo que activa rutas de señalización involucradas en la respuesta celular. Esto ha generado una nueva era de inmunoterapia, en la que se usan moléculas miméticas de sus originales en bacterias6 o se utilizan fracciones inmunogénicas derivadas de microorganismos.
El Ribovac, Ribomunyl e Immunocytal, que en delante abreviaremos “R”, son nombres comerciales para el mismo inmunoestimulante ribosomal compuesto de extractos ribosomales de cuatro bacterias (Diplococcus pneumoniae, Staphylococcus pyogenes, Klebsiella pneumoniae y Haemophyllus influenzae) y proteoglicanos de K. pneumoniae, estos últimos considerados como adyuvantes naturales que potencian la inmunogenicidad de las fracciones ribosomales y además poseen propiedades inmunoestimulantes7.
Este trabajo se realizó con el objetivo de comparar la respuesta celular inducida por dosis con capacidad inmunoestimulante reconocida de R en células mononucleadas humanas de sangre periférica.
Material y métodos
Se obtuvieron 10 ml de sangre heparinizada proveniente de tres donantes sanos adultos. Se aislaron células mononucleadas en gradientes de Ficoll-Paque premium (d=1,077). Se estimularon con concentraciones variables de R que en ensayos previos demostraron desencadenar una potente respuesta de producción de anticuerpos y otros factores solubles. El control negativo no llevó estímulo. Las células se incubaron en RPMI-1640 (Roswell Park Memorial Institute) y suero fetal 10% con 95% de humedad y 5% de CO2 y se estudió a las 4 y 6 horas, el efecto de las fracciones ribosomales a las concentraciones siguientes: 3.9; 7.8; 15.6; 31,2 y 62,5 mg/ml, sobre la expresión de moléculas de superficie de leucocitos con la combinación de anticuerpos monoclonales CD3/CD16 & CD56 FITC1PE Exp. Beckman Coulter Inc. Fullerton CA. USA.,CD3/19/45 FITC/PE/PECy5 Exp. Beckman Coulter Inc. Fullerton CA. USA. Las subpoblaciones de células mononucleadas estimuladas por R se identificaron con un clitómetro de flujo EPICS Xcl, BECKMAN COULTER, USA.
El efecto de R sobre la proliferación de células mononucleadas se midió a las 72 horas de cocultivo de estas con las concentraciones de R antes mencionadas en sobrenadantes de cultivo a los tiempos de incubación: 4 h, 6 h, 24 h y 72 h. Se utilizaron Kits de ELISA de la marca BIOSOURCE (Invitrogen Corp. Carlsbad, CA, USA).
Para evaluar la viabilidad de las células mononucleadas se usó el método de exclusión de azul de tripano al 4%.
Se analizaron los datos en el programa Microsoft Excel y el programa estadístico SPSS versión 18. Los procedimientos estadísticos descriptivos e inferenciales que se emplearon incluyeron porcentajes, medias, error estándar y t de Student. Se aceptó para las mediciones un nivel de significación p<0,05. Los experimentos se realizaron por triplicado.
Resultados
La curva de calibración del ensayo ELISA que se usó para realizar las determinaciones de IL-6 en sobrenadantes de cultivo tuvo como ecuación (y = 0,0129x + 0,0873; R2=0,9975). Al comparar la expresión de IL-6 en el tiempo entre sobrenadantes de células mononucleadas que habían sido tratados por 6 horas, 24 horas y 72 horas con concentraciones variables de R se encontró que los efectos más constantes de elevación de niveles de IL-6 se obtuvieron a las 24 horas para las concentraciones 3,9, 7,8, 15,6, 31,2 y 62,5 mg/ml de R aunque no fueron estadísticamente significativos.
Los niveles de IL-6 tendieron a disminuir para todas las concentraciones estudiadas respecto del control con células no tratadas al tiempo 72 horas, este cambio fue estadísticamente significativo al comparar células no tratadas con células tratadas a una concentración de 31.2 mg/ml de Ribovac®, (p=0.006).
Expresión del marcador CD3 por células mononucleadas estimuladas con Ribovac®
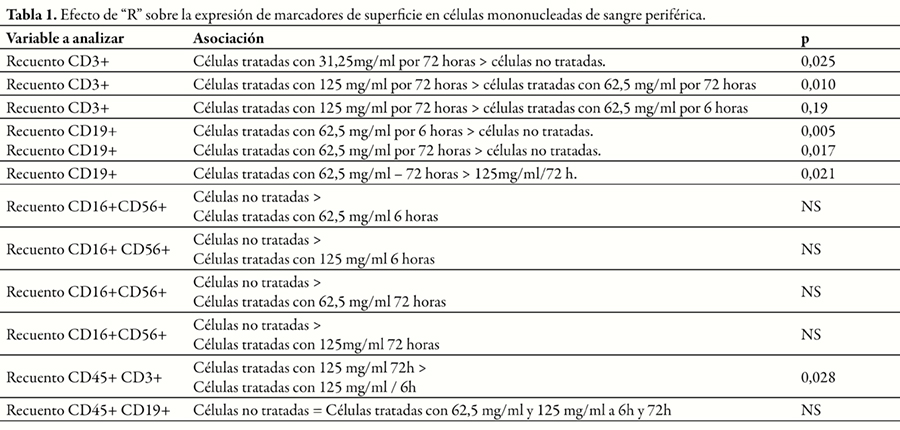
Se obtuvieron valores máximos de conteo de células CD3+ en células mononucleadas tratadas por 72 horas con concentraciones de 62,5 μg/ml de R (CD3 basal a las 72 horas vs. CD3 62,5 mg/ml a las 72 horas; p=0,025) (Tabla 1).
También se encontraron valores estadísticamente significativos al comparar los recuentos de células CD3+ entre células mononucleadas tratadas por 72 horas a concentraciones de 62,5 mg/ml respecto de aquellas tratadas en el mismo tiempo pero a concentraciones de 125 mg/ml, p=0,010 y entre la expresión CD3 en células tratadas con 62,5 mg/ml de R por 6 horas respecto a expresión de CD3 en células tratadas con 125 mg/ml de R a las 72 horas (p=0,019). En todos los casos se obtuvieron los efectos máximos en células tratadas con la concentración de 125 mg/ml de R (Tabla 1).
Se encontró un coeficiente de correlación R2=0,773 al evaluar la expresión de CD3 en células tratadas por 72 horas con 125 mg/ml y la encontrada a la misma concentración pero en un tiempo de 6 horas, de forma que la magnitud de la asociación entre la expresión de CD3 por células mononucleadas depende también del tiempo de estimulación y no solo de la dosis aplicada de R.
Al comparar la expresión de CD19 inducida por concentraciones evaluadas de Ribovac® se obtuvo: CD19 [basal] < CD19 [62,5 mg/ml] (t=6 horas; p=0,005); CD19 [basal] < CD19 [62,5 mg/ml] (t=72 horas; p=0,017); CD19 [62,5 mg/ml] > CD19 [125 mg/ml] (t=72 horas; p=0,021) (Tabla 1).
El número de células CD16+CD56 + fue menor en células tratadas con las concentraciones 62,5 y 125 mg/ml de R respecto a células no tratadas; aunque esta disminución no fue significativa estadísticamente respecto del tiempo de estimulación ni de la dosis usada de R al comparar tanto la media de los recuentos de células CD16+CD56+ como la intensidad media de fluorescencia, entre células tratadas con R y controles no tratados (Tabla 1).
No se encontraron diferencias significativas al comparar la expresión de CD45 entre células tratadas y no tratadas ni entre células tratadas con diferentes concentraciones de R. Este cambio no fue significativo respecto del tiempo de estimulación ni de la dosis administrada de R. Se encontró un aumento de la población celular que coexpresó CD45+ y CD3+ del 76%, el cual fue directamente proporcional al tiempo de estimulación, al comparar células tratadas con 125 mg/ml a las 6 horas y a las 72 horas (p=0,028; R2=0,766).
La coexpresión de CD45 y CD19 por células mononucleadas no varió en forma estadísticamente significativa respecto del tiempo de tratamiento ni de la concentración de R usada, al comparar células tratadas a diferentes concentraciones de R entre sí y entre estas células con aquellas no tratadas.
Discusión
R estimula la repuesta inmune inespecífica a través de la estimulación de la actividad de macrófagos, polimorfonucleares y células natural killers (NK)8,9 y se ha documentado la producción de IL-6 por linfocitos humanos de sangre periférica cuando se estimulan con proteoglicanos de membrana de K. pneumoniae (0,01 a 100 mg/ml)10. Estos proteoglicanos también inducen en monocitos humanos de sangre periférica la producción de IL-8 y de factores quimiotácticos de monocitos.11
En una comunicación se menciona el efecto de R en el aumento en la producción de citocinas proinflamatorias (IL-1, IL-6, IL-8) (Clot J., 1997)5. En concordancia con esa comunicación, en este estudio se encontró un aumento en la producción de IL-6 por células mononucleadas a las 24 horas de tratamiento con dosis variables de Ribovac® y luego los valores de IL-6 decrecieron a las 72 horas, de forma que su síntesis puede ser autorregulada en un tiempo corto porque a las 72 horas los niveles de IL-6 fueron similares a los basales (sin estimulación). No tenemos una explicación para este fenómeno de inmunorregulación pero en estudios realizados previamente en nuestro laboratorio hemos encontrado que en sujetos normales la expresión de IL-6 puede regularse localmente por el sitio en que ocurre la respuesta que desencadenó su síntesis y que ésta suele regularse en un corto tiempo (datos enviados a publicación).
Se ha reportado el efecto de R en la activación de algunas de las funciones de las células linfoides, en la estimulación de la producción de radicales libres del oxígeno, en la quimiotaxis y en la adhesión5 lo cual está en relación con la eficacia de la inmunoterapia con R, la cual ha sido documentada por varios ensayos clínicos en niños y adultos con IRVRA12.
En este estudio encontramos cambios a las 72 horas en la expresión de los marcadores CD3 y CD19 de células mononucleadas estimuladas con R y que este estímulo fue máximo a la concentración de 125 mg/ml de R lo cual muestra que R induce la expansión de poblaciones de linfocitos, en particular células B a las 72 horas. Esto concuerda con el hecho de que R induce una potente producción de anticuerpos específicos en ratones y humanos [8,9,13]. Una vez que los linfocitos B efectores son estimulados, migran a sitios de mucosa en donde se diferencian e inducen la síntesis de IgA, allí son detectables unidades formadoras de anticuerpos específicos.14,15 En este estudio la expresión de CD3 y CD45 fue máxima a las 72 horas de tratamiento de las células con 125 mg/ml de R lo cual apoya el hecho de que ocurre una expansión clonal de linfocitos dependiente de los ribosomas bacterianos y proteoglicanos presentes en R, lo cual unido al hecho de que no se apreció un aumento en la coexpresión de CD45 y CD19, sugiere que la expansión de células T es medible en término de incrementos de conteos celulares y que en la población de células B parece ser más importante el cambio hacia fenotipos efectores con mayor capacidad para producir anticuerpos. En próximos estudios es recomendable cuantificar células plasmáticas y usar marcadores de activación de célula B para demostrar el fenómeno de cambio de linfocito B a un inmunofenotipo más maduro producto de la estimulación con R y correlacionar estos cambios con la respuesta de anticuerpos específicos.
Desde hace más de 20 años se ha documentado que la combinación de proteoglicanos de membrana y ribosomas estimula funciones citotóxicas y no citotóxicas de células NK16. En este estudio encontramos que R indujo una disminución no significativa del total de células CD16+CD56+. Este cambio debe interpretarse en el contexto de la coexpresión de otros marcadores de citotoxicidad y citoadhesión de células NK. Si consideramos que la mayoría de las células CD16+CD56+ fueron CD3– (inmunofenotipo NK), es entonces recomendable separar la expresión de CD16 de la de CD56 para evaluar la capacidad citotóxica de las células NK, lo cual es una limitación del presente estudio. A pesar de no haberse detectado cambios en el número de células NK, puede existir una maduración en la respuesta de éstas, lo cual se relaciona con la sobreexpresión de IL-6 encontrada en este estudio y con el aumento de la actividad NK reportada por otros autores (Allavena et al. 1989)16.
Conclusiones
Ribovac® tiene un efecto dependiente de dosis y tiempo de exposición en la expresión de IL-6 por células mononucleadas cultivadas con diferentes concentraciones de Ribovac® en tiempos de 4 h, 6 h, 24 h y 72 h.
La expansión de poblaciones linfoides y la maduración de estas hasta inmunofenotipos con mayor capacidad efectora debe tomarse en cuenta a la hora de decidir el tiempo y repetición de dosis de Rivobac® en personas con IRVRA, es importante evaluar el impacto que tiene la inmunocompetencia del huésped sobre la eficiencia de Rivobac®.
Agradecimientos
Este trabajo fue parcialmente financiado por el proyecto RIBO-MEX-001-08 el cual recibió fondos de laboratorios Pierre Fabre México.
Al matemático Carlos Gómez Alonso del Centro de Investigaciones Biomédicas de Occidente del Instituto Mexicano del Seguro Social en Morelia, Michoacán. México por el apoyo en la estadística.
Al Dr. Sergio Guerrero, encargado del citómetro de flujo de la División de Estudios de Posgrado Facultad de Ciencias Médicas y Biológicas “Dr. Ignacio Chávez” de la Universidad Michoacana de San Nicolás de Hidalgo, Morelia, Michoacán, México, por el apoyo en la interpretación de los datos de citometría.
<
-
Robaina Suárez G, Campillo Molieva R. Morbilidad y manejo de infecciones respiratorias agudas en menores de 5 años. Rev Cubana Pediatr [revista en la Internet]. 2003 Sep [citado 2011 Mar 26]; 75(3): Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0034-75312003000300007&lng=es
-
Álvarez Castelló M, Castro Almarales R, Abdo Rodríguez A, Orta Hernández SD, Gómez Martínez M, Álvarez Castelló M del P. Infecciones respiratorias altas recurrentes: Algunas consideraciones. Rev Cubana Med Gen Integr [revista en la Internet]. 2008 Mar [citado 2011 Mar 26]; 24(1):. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864-21252008000100011&lng=es.
-
Nelson H. Advances in upper airway diseases and allergen immunotherapy. J Allergy Clin Immunol 2005;115:676-684.
-
Akdis M, Akdis CA. Mechanisms of allergen-specific immunotherapy. J Allergy Clin Immunol 2007;119:780-789.
-
Clot J. Pharmacology of Ribosomal Immunotherapy. Drug 1997;54:33-36.
-
Bocaccio C, Jacod S, Kaiser A, Boyer A, Abastado JP, Nardin A. Identification of a clinical-grade maturation factor for dendritic cell. J Immunother 2002;25(1):88-96.
-
Donnelly JJ, Deck RR, Liu M A. Immunogenicity of a Hemophilus Influenzae polysaccharide-Neisseria meningitides outer membrane protein complex conjugate vaccine. J. Immunol 1990;145:3071-3079.
-
Fontages R, Robert D, Content Y, Nis G. Pouvoir vaccinant de ribosomes extrait de K. pneumoniae, D. pneumuniae, Streptococcus pyogenes, Haemophilus influenzae et d´une fraction membranaire de K. pneumonia. Rev Fr d´Allergol 997;17:35-81.
-
Fontages R, Robert D, Content Y. Study of the immunogenicity of ribosomes and riboso-mal RNA extracted from K. pneumonia and S. pneumonia. Arzneimittelforschumg 1980;30: 14272.
-
Sironia M, Sicaa A, Rigantia F, Licciardello L, Colottaa F, Mantovani A. Interleukin-6 gene expression and production induced in human monocytes by membrane proteoglycans from Klebsiella pneumoniae International Journal of Immunopharmacology 1990;12(4):397-402
-
Luini W, De Rossi M, Licciardello L, Francesco Colotta and Alberto Mantovani. Chemotactic cytokine gene expression and production induced in human monocytes by membrane proteoglycans from Klebsiella pneumonia. Int Immunopharmacol 1991;13:631-637.
-
Bellanti JA, Olivieri D, Serrano E. Ribosomal immunostimulation: Assessment of studies evaluating its clinical relevance in the prevention of upper and lower respiratory tract infections in children and adults. BioDrugs 2003;17(5):355-367.
-
Michel FB, Dussourd D´Hinterland L, Bousquet J, Pinel Am, Normier G. Immunostimulant by a ribosomal vaccine associated with a bacterial cell wall-adjuvant in humans. Infect Immun 1978;20:760-769.
-
Fauré GC, Bené MC, Simon C. Increase in specific antibody-forming cells in human tonsils after oral stimulation with D-53, a ribosomal vaccine. Int J Immunopharmacol 1990;12(3):315-320.
-
Béné MC, Kahl L, Perruchet AM, Hermes H, Mosgues M, Normier G, Binz H, Faure GC. Bacterial lysates and ribosomes as inducers of specific immune responses: a comparative study. Scand J Immunol 1993;38(5):496-498
-
Allavena P, Annalaura E, Pirelli A, Licciardello L, Mantovani A. Stimulation of citotoxic and non-cytotoxic functions of natural killer cell by bacterial membrane proteoglycans and ribosomes. Int J Immunopharmacol 1989;11(1):29-34.
Texca Tatevari Méndez-López
Laboratorio de Inmunología, División de estudios de posgrado, Facultad de Ciencias Médicas y Biológicas “Dr. Ignacio Chávez”, Universidad Michoacana de San Nicolás de Hidalgo, Morelia, Michoacán, México..
Alain Raimundo Rodríguez-Orozco
Laboratorio de Inmunología, División de estudios de posgrado, Facultad de Ciencias Médicas y Biológicas “Dr. Ignacio Chávez”, Universidad Michoacana de San Nicolás de Hidalgo. Instituto de Investigación Científica en Temas de Familia, Alergia e Inmunología, Morelia, Michoacán, México..
Carlos Béjar Lozano
Laboratorios SERVIMED. Morelia. Michoacán, México.
Autor correspondencia
Alain Raimundo RodrÃguez-Orozco
Laboratorio de InmunologÃa, División de estudios de posgrado, Facultad de Ciencias Médicas y Biológicas “Dr. Ignacio Chávezâ€, Universidad Michoacana de San Nicolás de Hidalgo. Instituto de Investigación CientÃfica en Temas de Familia, Alergia e InmunologÃa, Morelia, Michoacán, México..
Correo electrónico: arorozco69@yahoo.com.mx
Para descargar el PDF del artículo
Efecto comparado de dosis inmunoestimulantes de fracciones ribosomales y proteoglicanos de membrana sobre la activación de subpoblaciones de células mononucleadas humanas de sangre periférica
![]() Haga click aquí
Haga click aquí
Para descargar el PDF de la revista completa
Archivos de Alergia e Inmunología Clínica , Volumen Año 2012 Num 1
Archivos de Alergia e Inmunología Clínica
Número 1 | Volumen
43 | Año 2012
Editorial
Comité Editorial
Anafilaxia a leche de vaca. Tratami...
Mónica Sanabria y cols.
Efecto comparado de dosis inmunoest...
Texca Tatevari Méndez-López y cols.
Efectos de la inmunoterapia sobre l...
Nelly Barrera y cols.
Polen y cenizas en Buenos Aires
Laura Barrionuevo y cols.
Etiquetas
ribosomas bacterianos, proteoglicanos de membrana, infecciones respiratorias recurrentes, inmunoestimulación, células mononucleadas, CD3, CD19, CD45, CD16 CD56, CD19, IL-6, Ribovac, Ribomunyl, Immunocytal
Tags
bacterial ribosomes, membrane proteoglycans, recurrent respiratory infections, immune stimulation, mononuclear cells, CD3, CD19, CD45, CD16 CD56, CD19, interleukin 6, Ribovac, Ribomunyl, Immunocytal
Efecto comparado de dosis inmunoestimulantes de fracciones ribosomales y proteoglicanos de membrana sobre la activación de subpoblaciones de células mononucleadas humanas de sangre periférica
Autores
Texca Tatevari Méndez-López, Alain Raimundo Rodríguez-Orozco, Carlos Béjar Lozano
Publicación
Archivos de Alergia e Inmunología Clínica
Editor
Asociación Argentina de Alergia e Inmunología Clínica
Fecha de publicación
Registro de propiedad intelectual
© Asociación Argentina de Alergia e Inmunología Clínica